电话咨询
400-811-6667微信公众号

微信公众号
访问手机版

访问手机版
我国科研团队开创性利用干细胞疗法成功实现1型糖尿病的功能性治愈。
在探索诱导性多能干细胞(iPSC)治疗重大疾病的前沿领域,我国科学家取得了历史性的突破。他们首次运用干细胞再生疗法,成功实现了一名1型糖尿病患者的功能性治愈。
这一成果由天津市第一中心医院的沈中阳、王树森研究组,携手北京大学、昌平实验室的邓宏魁研究组,以及杭州瑞普晨创科技有限公司共同打造。他们通过创新的化学重编程技术诱导多能干细胞制备胰岛细胞,并成功地将这些细胞移植给了一名1型糖尿病的患者。该研究成果在9月25日晚在国际权威期刊《细胞》上发表。
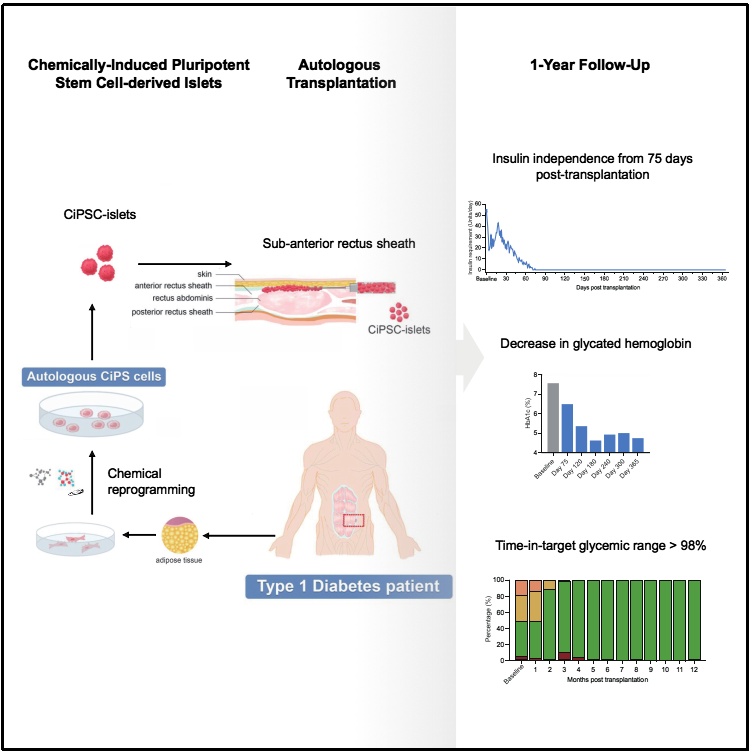
据天津市第一中心医院的王树森主任介绍,糖尿病作为威胁人类健康的重大疾病之一,其中1型糖尿病是较为严重的一种。现有的治疗方法难以实现对血糖的精确调控,从而容易引发多种并发症,严重影响患者的生活质量。尽管胰岛移植在临床疗效上取得了一定进展,但胰腺供体的稀缺性却极大地限制了其广泛应用。而利用人诱导性多能干细胞制备的胰岛细胞,有望为这一难题提供新的解决方案。

多能干细胞(Pluripotent stem cell,PSC)因其具有自我更新和分化成功能细胞类型的能力,多能干细胞具有分化出多种细胞组织的潜能,因此作为无限的细胞来源,在诸如胰岛移植等细胞替代疗法中显示出巨大潜力。
多能干细胞制备的胰岛细胞为糖尿病移植治疗开辟了新的道路,这些细胞凭借其无限增殖的特性,能够分化成生物体内所需的绝大多数功能细胞类型,从而成为治疗糖尿病等疾病的理想选择。事实上,多能干细胞因其强大的再生能力,被誉为再生医学中最具潜力的“种子细胞”。
邓宏魁教授团队在2013年《科学》杂志上发表了一项革命性的研究成果:他们提出了一种全新的诱导人多能干细胞制备技术——化学重编程。这项技术仅利用外源性化学小分子,就实现了细胞命运的逆转,成功地将小鼠体细胞重编程为多能干细胞(简称CiPS细胞)。这一发现不仅简化了多能干细胞的制备过程,还极大地提高了其制备效率。
在此基础上,邓宏魁教授团队的研究并未止步。2022年,他们在《自然》杂志上发表了进一步的研究成果:利用化学小分子成功地将人成体细胞诱导为多能干细胞(人CiPS细胞)。这一成果标志着多能干细胞研究领域又取得了重大突破,为未来的医学研究和治疗提供了更多的可能性和希望。
这名患者已患有1型糖尿病11年,完全依赖胰岛素治疗,但血糖控制效果并不理想,多次出现严重低血糖症状。然而,在接受移植后,患者的血糖调控能力得到了恢复,呈现出内源自主性和生理性的特点。在移植后的75天内,患者完全摆脱了胰岛素注射治疗,并持续保持了一年以上的良好状态。目前,患者的各项糖尿病相关指标均已恢复正常水平,实现了1型糖尿病的临床功能性治愈。
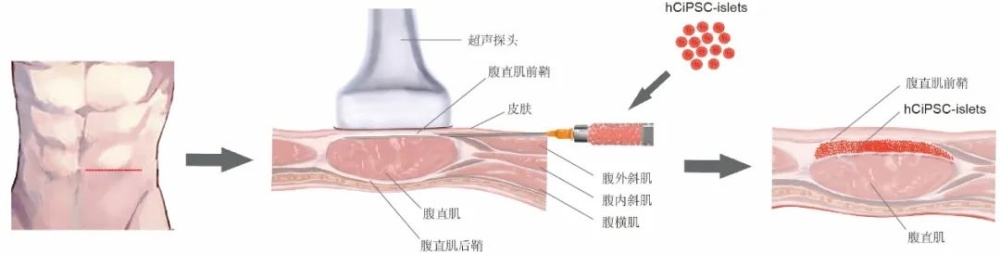
北京大学干细胞研究中心主任邓宏魁教授介绍,多能干细胞具有无限增殖和分化为生物体所有功能细胞类型的潜力,是再生医学领域的核心“种子细胞”。研究团队通过化学小分子调控的手段,成功地将人体细胞诱导为多能干细胞,开辟了全新的多能干细胞制备途径。该技术也因此荣获了2024年未来科学大奖的“生命科学奖”。
邓宏魁教授还表示,化学重编程技术制备的功能细胞在临床治疗疾病上取得的初步成功,预示着该技术有望成为高效制备各种功能细胞类型的通用底层技术,为细胞治疗在重大疾病治疗中的广泛应用开辟了崭新的道路。
这位天津女子的成功案例,无疑为我们展示了重编程干细胞在糖尿病治疗中的巨大潜力。它不仅为患者带来了新的希望,更为医学界开辟了一条全新的治疗路径。
我们相信,在不久的将来,随着科技的不断进步和研究的深入,越来越多的糖尿病患者将能够摆脱疾病的困扰,重新拥抱健康、美好的生活。让我们一起期待这个美好的未来吧!