电话咨询
400-811-6667微信公众号

微信公众号
访问手机版

访问手机版
2024年8月27日,中国医疗健康领域传来重大喜讯——传奇生物(NASDAQ:LEGN)递交的西达基奥仑赛注射液(Carvykti)的新药上市申请,正式获得了中国国家药监局(NMPA)的批准。这标志着我国在多发性骨髓瘤(MM)治疗领域迈出了重要一步,为无数患者开启了前所未有的治疗可能,点亮生命的科技之光。
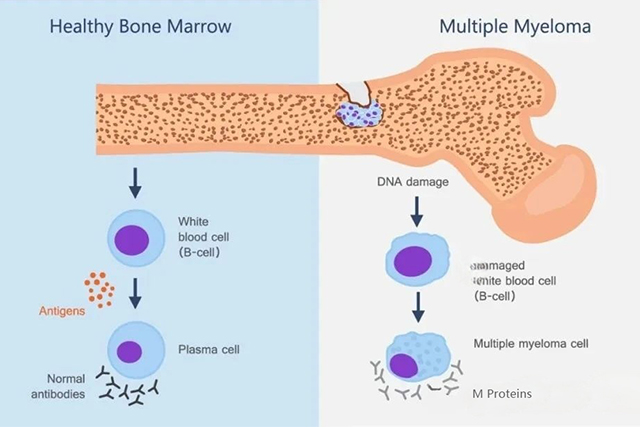
根据中国国家药监局(NMPA)官网最新公示,传奇生物递交的西达基奥仑赛注射液的新药上市申请已正式获批。该产品本次获批适应症为:用于治疗既往接受过一种蛋白酶体抑制剂和一种免疫调节剂治疗后复发或难治性(R/R)多发性骨髓瘤(MM)成人患者。CARTIFAN-1 临床试验主要研究者陈赛娟院士表示:多发性骨髓瘤(MM)是一种无法治愈的恶性浆细胞肿瘤,约占血液恶性肿瘤的10%2,患者终将面临复发,且随着复发次数增多,治疗难度也随之增加,患者的缓解质量更差,无进展生存期(PFS)和复发后的生存时间越短。对于中国MM患者来说,西达基奥仑赛的获批为临床医生提供了创新、安全可控的有效的疗法。西达基奥仑赛在临床开发研究中已展现出良好的临床疗效,在多线治疗失败的复发、难治的MM患者中能产生早期、深度且持久的缓解,以及更长的PFS生存获益。这对于骨髓瘤患者来说是一个重大利好消息,我们期待这一新型治疗方案能够为更多患者带来生存的希望,改变目前的骨髓瘤患者治疗格局。

此次获批是基于在国内进行的一项多中心确证性Ⅱ期临床研究CARTIFAN-1(NCT03758417),旨在评估西达基奥仑赛注射液在既往接受过至少三线治疗(包括至少一种蛋白酶体抑制剂和至少一种免疫调节剂)的复发或难治性多发性骨髓瘤患者中的疗效及安全性。值得关注的是,西达基奥仑赛此前已在美国、欧盟、日本等多个国家和地区获批上市,其疗效与安全性广受好评。在美国,它成为复发或难治性多发性骨髓瘤患者治疗领域的新希望,为患者提供了前所未有的治疗机遇。此次国内获批,标志着该药物的应用范围将进一步拓展,为中国患者带来更加多样化的治疗选择,助力更多患者重获健康。
随着西达基奥仑赛在国内成功获批,我国CAR-T细胞疗法市场将迎来更加广阔的发展空间。目前,国内已有包括西达基奥仑赛在内的多款CAR-T产品获批上市,为患者提供了多元化的治疗选择。未来,随着技术的不断进步和临床应用的深入探索,CAR-T细胞疗法必将在更多医疗领域绽放光芒,成为患者重拾健康、重获新生的坚强后盾。